Содержание к диссертации
Стр.
ВВЕДЕНИЕ 4
1. ОБЗОР ЛИТЕРАТУРЫ 8
Метаболизм метионина 8
1.1 Биологические реакции
трансметилирования 12
Другие Ме1(Аёо)-зависимые процессы 15
Биологическая роль и применение S-метилметионина 18
Катаболизм метионина 20
Регулирование обмена метионина фосфорорганическими аналогами серосодержащих аминокислот 21
Микробная L-метионин-у-лиаза 27
2. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ 38
Синтез фосфорорганических аналогов у-замещенных серосодержащих аминокислот 38
Стабильность фосфорорганических аналогов S-аденозилметионинаи S-метилметионина 42
Синтез фосфорорганических аналогов гомосерина 47
Взаимодействие фосфорорганических аналогов аминокислот обмена метионина с L-метионин-у-лиазой 50
Энантиоселективный синтез фосфиновых аналогов у-замещенных серосодержащих аминокислот 65
Влияние фосфинового аналога метионина на клетки
Citrobacter intermedins 68
3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ 73
Препараты и оборудование 73
Синтез фосфорорганических аналогов серосодержащих аминокислот 74
Исследование устойчивости фосфорорганических аналогов S-аденозилметионина и S-метилметионина 79
Синтез фосфорорганических аналогов гомосерина 80
Взаимодействие фосфорорганических аналогов аминокислот с L-метионин-у-лиазой из С. intermedins и С. freundii 83
Энантиоселективный синтез фосфиновых аналогов у-замещенных серосодержащих аминокислот 85
Влияние фосфинового аналога метионина на клетки
Citrobacter intermedins 87
ВЫВОДЫ 88
ЛИТЕРАТУРА 89
Введение к работе
Обширное семейство природных и синтетических
фосфорорганических аналогов аминокислот включает большую группу соединений, относящихся к фосфиновым 1 и фосфоновым 2 кислотам, в основе разнообразной физиологической активности которых лежит влияние на обмен аминокислот и особенности действия которых во многом зависят от строения фосфорсодержащего фрагмента.
R'
В 1-аминоалкилфосфонатах 2 двухосновная фосфонатная группа Р(0)(ОН)2 значительно отличается размерами, геометрией и кислотностью от карбоксильной группы аминокислоты, что делает представления о прямом структурном подобии фосфонатов 2 аминокислотам достаточно формальными. Вместе с тем, строение фосфонатов 2 позволяет рассматривать их как стабильные аналоги лабильных переходных состояний или промежуточных соединений в ферментативных превращениях аминокислот, что явилось основой создания новых видов ингибиторов ферментов аминокислотного обмена [1] и гаптенов для каталитических антител [2].
Модификация фосфонатного фрагмента с заменой гидроксильной группы на водород вызывает кардинальные изменения базовых биохимических характеристик фосфоаналогов. Исследования по взаимодействию фосфинатов 1 с ферментам обмена аминокислот показали, что введение одноосновной группы Р(0)(ОН)Н вместо
карбоксильной группы аминокислоты не сказывается качественно на
связывании аналогов 1, но приводит к существенному снижению
скоростей субстратных превращений [3]. Изучение биологической
активности этих аналогов показало, что они способны, подобно
аминокислотам, к транспорту через микробные клеточные стенки [4].
Существенно, что способность фосфинатов 1 к субстратным
превращениям и образованию в качестве продуктов новых
фосфорорганических соединений оказалась связанной с их биологической
активностью. Таким образом, аминоалкилфосфинаты 1 могут
рассматриваться как изостеры природных аминокислот и являются
перспективным источником химических инструментов для
энзимологических исследований и биологически активных веществ.
Однако до настоящего времени не было осуществлено систематического
изучения их свойств как аналогов субстратов ферментов обмена
аминокислот, в особенности тех, коферментом которых является
пиридоксаль-5'-фосфат (PLP). О
NH2 NH2
la Y=SCH3,X=H lr R=Ado, X=H, Y=C1
2a Y=SCH3, X=OH 26 R=Ado, ХЮН, Y=OAc
16 Y=SH, X=H Ід R=CH3, X=H, Y=I
luY=SAdo,X=H 2b R=CH3, X=OH, Y=I
їж Y=OH, X=H le R=CH3, X=H, Y=OTs
2д Y-OH, X=OH 2r R=CH3, X=OH, Y=OTs
В настоящей работе основными химическими объектами исследования были фосфиновые и фосфоновые аналоги аминокислот обмена метионина (la-ж, 2а-д), что определялось значимостью процессов биометилирования в клеточном метаболизме, а также активностью подобных веществ, как антибактериальных агентов, ингибиторов роста
опухолевых клеток и эффективных фунгицидов [4-6]. Энзимологические исследования проводились на ферменте катаболизма метионина - PLP-зависимой L-метионин-у-лиазе, регулирование активности которой рассматривается как перспективное направление дизайна селективных антимикробных агентов [7].
Целью настоящей работы являлось выявление и изучение свойств фосфиновых и фосфоновых аналогов метионина и родственных веществ, определяющих особенности их химического поведения и взаимодействия с биологическими объектами на примере L-метионин-у-лиазы и клеток Citrobacter intermedins - продуцента этого фермента
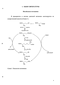
В соответствии с целью и задачами исследования в Литературном обзоре обсуждаются основные реакции метаболизма метионина и S-аденозилметионина (Met(Ado)) и некоторые способы их химического регулирования. Особое внимание уделено рассмотрению свойств микробной PLP-зависимой L-метионин-у-лиазы и обсуждению возможностей использования фосфорорганических аналогов серосодержащих аминокислот для воздействия на метионин- и Met(Ado)-зависимые процессы.
Постановка задачи и результаты исследования являются приоритетными, их научная новизна и практическая ценность состоит в следующем:
Найдены и исследованы новые свойства фосфорорганических аналогов S-аденозилметионина - эффективных биорегуляторов Met(Ado)-зависимых процессов. Разработан оригинальный способ получения фосфинового и фосфонового аналогов гомосерина из фосфорорганических аналогов S-метилметионина.
Найдено, что фосфорорганические аналоги метионина эффективно связываются с PLP-зависимой L-метионин-у-лиазой и являются конкурентными ингибиторами фермента. Показано, что фосфиновые
аналоги метионина и гомосерина претерпевают медленные субстратные превращения под действием фермента в фосфиновый аналог кетобутирата. Установлено, что стереохимия ферментативной реакции сохраняется в случае фосфиновых аналогов аминокислот. Исследованы спектральные свойства комплексов фосфинового и фосфонового аналогов метионина с L-метионин-у-лиазой.
Для фосфинового аналога метионина исследована рН-зависимость кинетических параметров реакции а,у-элиминирования. Установлено, что форма зависимости и оптимальные значения рН для ферментативной реакции сохраняются при переходе от природного субстрата к его фосфиновому аналогу.
Предложен химико-энзимологический метод синтеза оптически активных фосфиновых аналогов серосодержащих аминокислот.
Впервые показано, что фосфиновый аналог метионина способен индуцировать биосинтез L-метионин-у-лиазы в клетках С. intermedins подобно природной аминокислоте.
Проведенные исследования демонстрируют перспективность использования аналогов для тонкого химического регулирования обмена серосодержащих аминокислот и представляют интерес для изучения механизма действия PLP-зависимых ферментов, выяснения зависимости каталитических свойств от строения и кислотно-основных свойств ионизируемых групп субстрата,
Отдельные части диссертации были представлены на Всероссийской конференции «Проблемы медицинской эшимологии» (Москва, Россия, 2002), на 3-м съезде Биохимического общества (Санкт-Петербург, Россия, 2002), на 5-й международной Школе-конференции «Green Chemistry» (Венеция, Италия, 2002).