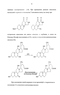Содержание к диссертации
Введение
ГЛАВА I. Синтез и биологическая активность некоторых стероидов типа желчных кислот(литературный обзор) 9
1.1. Синтез и свойства ряда производных холановых кислот 10
1.2. Определение содержания холановых кислот в биологических объектах методом газожидкостной хроматографии 19
1.3. Исследование литолитических свойств некоторых производных холановых кислот 21
ГЛАВА II. Исследование реакций протекающих по карбоксильной, гидроксильной, кетонной и аминнай группам в ряду холановых кислот (обсуждение результатов) 29
2.1. Синтез и химические свойства сложных эфиров холановых кислот 31
2.2. Изучение реакции гидрозидирования холановых кислот 53
2.3. Синтез и свойства аминотиофенсодержащих холановых кислот 56
ГЛАВА III. Исследование возможных областей применения некоторых синтезированных соединений 66
3.1. Исследование препаратов, растворяющих холестериновые камни желчного пузыря 66
3.2. Флотационные свойства некоторых солей холановых кислот 74
3.3. Влияние За,7а-дигидроксихолановой кислоты на физико-химические свойства дестабилизированной желчи 74
ГЛАВА IV. Экспериментальная часть 83
Выводы 94
Литература
- Определение содержания холановых кислот в биологических объектах методом газожидкостной хроматографии
- Исследование литолитических свойств некоторых производных холановых кислот
- Изучение реакции гидрозидирования холановых кислот
- Влияние За,7а-дигидроксихолановой кислоты на физико-химические свойства дестабилизированной желчи
Введение к работе
Актуальность работы. Стероидные соединения чрезвычайно широко распространены в природе. В организме растений и животных содержатся стероиды, играющие важную роль в их жизнедеятельности. В последние годы получено большое количество стероидных соединений из природных источников, а также синтетическим путём.
В химическом отношении стероиды являются производными углеводорода 1,2-циклопентанопергидрофенантрена.
Удлинение боковой цепи при Си приводит к желчным кислотам (холановым кислотам), играющим значительную роль в процессах пишеварения; представителем их является холевая кислота.
Среди многих физиологически активных стероидов важное место занимают холановые кислоты. Особий интерес представляют производные За,7а,12а-тригидрокси-, За,7а-дигидрокси-, За,12а-дигидрокси-, За-гидрокси и За,7а,12а-трикетохолановых кислот, которые содержат гидроксильные группы, легко окисляемые до кетогрупи, что даёт возможность синтезировать ряд производных холановых кислот, которые могут быть исходным сырьём для получения литолитических препаратов.
Несмотря на многообразие классов стероидных соединений, все они в настоящее время связаны между собой частичными синтезами, которые позволяют перейти от одного класса к другому путём усложнения или те упрощения структуры за счет введения, удаления или трансформации боковых цепей и функциональных заместителей.
Важно отметить, что в литературе имеются незначительные сведения о синтезе литолитических препаратов. Разработка наиболее приемлемых методик получения некоторых производных стероидов (в частности холановых кислот) на основе использования их карбоксильных, гидроксильных, кетонных, аминных и эфирных групп открывает новое
направление в органической химии, которое позволяет вести направленный синтез новых препаратов, растворяющих холестериновые желчные камни.
Учитывая все это можно сказать, что одним из способов модификации химической структуры холановых кислот, является проведения различных реакций протекающих по гидроксильной, карбоксильной и кетонной группам.
В связи с этим разработка удобных методов синтеза различных сложных эфиров, гидразидов, аминов - и N-аминотиофенсодержащих производных холановых кислот, а также модификации их структуры с целью получения новых биологически активных соединений, представляет собой актуальную задачу, как в плане развития органического синтеза, так и для практической медицины.
Цель исследования заключается в изучении поведения холановых
кислот в реакциях протекающих по карбоксильной, гидроксильной,
кетонной и аминной группам, в синтезе сложных эфиров, гидразидов и
аминотиофенсодержащих соединений, включающих
аминогетероциклического фрагмента, установлении строения образующихся продуктов, а также поиске путей практического использования синтезированных соединений.
Задачи исследования: -изучение реакции образования сложных эфиров холановых кислот; -синтез растворимых солей холановых кислот;
-разработка оптимальных условий реакции гидрозидирования холановых кислот;
-исследование реакции получения аминотиофенсодержащих холановых кислот и их поведения аминотиофенсодержащих холановых кислот в реакциях с различными арилсульфохлоридами, а также оптимизация
условий синтеза целевых продуктов в зависимости от природы реагента и
условий проведения реакции;
-изучения строения и физико-химических характеристик исходных
соединений, продуктов синтеза и их химических превращений;
-влияние За,7а-дигидроксихолановой кислоты на физико-химические
свойства дестабилизированной желчи;
-поиск путей практического применения синтезированных соединений.
Научная новизна: -впервые осуществлена реакция Гевальда в 12а-положении стероида в синтезе аминотиофенсодержащих холановых кислот; -проведена реакция взаимодействия аминотиофенсодержащих холановых кислот с арилсульфохлоридами, где было установлено, что ацильные и гидроксильные группы в положениях За,7а не затрагиваются; -изучены химические свойства этилового эфира-2' -амино-7,12-диоксо-, этилового эфира-2л-амино-12-окси-, этилового эфира-2"-амино-7,12-диокси- и этилового эфира-12-амино-3,7-диацетом етилхолат-2-ено[2,Зв]-тиофен-3'-карбоновой кислоты, установлено, что в реакциях протекают замещается один атом водорода в NH2- группе, -впервые исследовано поведение сложных эфиров холановых кислот в реакциях гидразидирования установлено, что выходы гидразидных соединений увеличиваются при использовании метиловых эфиров холановых кислот.
Практическая ценность: полученные натриевые соли За,7а,12а -тригидрокси- и За, 12а -дигидроксихоланових кислот предложены в качестве флотореагентов при флотации флюоритовых руд. -синтезированный За,7а-диацетопропилхолата можно использовать в качестве доступного сырья для получение препаратов растворяющих холестериновые желчные камни.
-дециловый эфир За,7а-дигидроксихолановой кислоты проявляет
способность растворять холестериновые желчные камни.
-пропиловый эфир За,7а-дигидрокси-12-кетохолановой кислоты
применяется в качестве внутреннего стандарта для определения желчных
кислот в биологических объектах методом газожидкостной
хроматографии.
Основные положения, выносимые на защиту: 1 .Синтезирован ряд сложных эфиров, растворимых солей, ацетатных, кетонных, гидразидов, аминотиофенсодержащих и других новых производных холановых кислот, содержащих циклопентанопер-гидрофенантреновый фрагмент. При этом в качестве второго компонента для конденсации нами подобраны соединения, которые известны как составные части лекарств и других биологически активных веществ. 2.Натриевые соли За,12а-дигидрокси-, За,7а,12а-тригидроксихолановой кислоты обладают высокими флотационными свойствами. 3. Дециловый эфир За,7а-дигидроксихолановой кислоты проявляет растворяющую способность холестериновых желчных камней.
Синтезированное соединение не оказывает токсического действия на лабораторных животных и на окружающие среды.
Исследовано влияние За,7а-дигидроксихолановой кислоты на физико-химические свойства дестабилизированной кислот.
Достоверность полученных результатов подтверждается следующим:
-высокой чувствительностью и специфичностью использованных химических, физико-химических и фармакологических, методов исследования;
-проведением систематической обработки полученных экспериментальных результатов общепринятыми методами.
Апробация работы. Основные результаты диссертационной работы были доложены на Республиканской конференции «Достижения в области химии и химической технологии» (Душанбе, 2001г.), Республиканской научно-практической конференции «Дастоварддои илми кимиё ва масоили таълимии он» посвященной 60-летию профессора Юсупова З.Н., (Душанбе, 2006г.), Республиканской научно-практической конференции «Актуальные вопросы семейной медицины» посвященной 75-летию член-корр. РАМН, проф. Ю.Б. Исхаки, (Душанбе, 2007г.).
Публикации. По теме диссертации опубликовано 5 научных статей и 3 тезиса докладов.
Структура и объём диссертации. Диссертация состоит из введения, четырёх глав, выводов, приложения, изложена на ПО страницах компыотерного набора, содержит 12 таблиц и 10 рисунков. Список использованной литературы включает 130 источников.
Определение содержания холановых кислот в биологических объектах методом газожидкостной хроматографии
Исследование содержания желчных кислот и их соотношения в желчи стало одним из высокочувствительных и информативных методов диагностики различных заболеваний печени и желчевыводящих путей. Болезни печени, занимающий значительное место в клинической патологии, сопровождаются нарушением одной из важнейших её функций: экскреции желчи, что приводит к значительному накоплению желчных кислот в желчи, а также к изменению их соотношения [34,35,36].
Определение содержания желчных кислот в желчи и в сыворотке крови методом газожидкостной хроматографии даёт точную информацию о характере болезни у больных с различными патологиями печени и желчсвыделительной системы [37,38,39].
Желчные кислоты (холановые кислоты) можно проанализировать полуколичественно с помощью тонкослойной хроматографии и количественно при высоком давлении с помощью газожидкостной хроматографии [40].
Для определения концентрации холановых кислот в растворе широко применяется метод ферментативного расщепления, который пригоден для диагностических целей [41,42]. Для более чувствительного определения в сыворотке применяются радиоиммуные методы, которые также пригодны для коммерческих целей [43].
Для выделения желчных кислот из водных растворов используют гидрофобные колонки [44]. Другие авторы [45] определяли желчные кислоты в виде трифторацетат производных. Некоторые данные свидетельствует об алитогенности желчи у собак, в силу чего эти животные не являются подходящими объектами для создания экспериментальной модели желчнокаменной болезни [46,47].
Это побудило других авторов провести сравнительное определение содержания желчных кислот в пузырной желчи собаки и человека методом газожидкостной хроматографии [48].
Ряд авторов, [49,50,51,52], газохроматографическим анализом определяли количество первичных и вторичных желчных кислот, рассчитывали их суммарное количество и их соотношение в желчи. Авторы сопоставляли результаты анализа содержания желчных кислот в пузырной желчи здоровых людей, больных холилитиазом в различной стадии его развития, с применением нового внутреннего стандарта и формулы рассчета.
Исследование содержания желчных кислот и их соотношения в сыворотке крови стало одним из высокочуствительных и информативных методов диагностики различных заболеваний печени и желчевыводящих путей. Болезни печени, занимающие значительное место в клинической патологии, сопровождаются экскрецией желчи, что приводит к значительному накоплению желчных кислот в сыворотке крови, а также к изменению в их соотношении.
Ряд исследователей [53,54,55] в сыворотке крови определяли методом газожидкостной хроматографии при таких условиях. Экстракция суммы конъюгированных и неконъюгированных желчных кислот. Затем гидролиз всех компонентов желчных кислот подвергали метилированию, образовавшиеся свободные желчные кислоты анализировали в газовом хроматографе типа "Хром-5" с пламенно-ионизационным детектором, при условии программирования температуры хроматографических колонок от 250-265С.
Исследование желчных кислот в биологических объектах, и в частности в сыворотке крови методом газожидкостной хроматографии, трудно из-за отсутствия вещества применяемого в качестве внутреннего стандарта.
Высше перечисленные авторы в качестве внутреннего стандарта использовали За,7а-дигидрокси-12-кетохолевую кислоту. В качестве объекта исследования использовали пузырную желч 15-здоровых людей, полученную при дуоденальном зондировании.
Таким образом, методом газожидкостной хроматографии авторами [55] было установлено, что в желчи 15-здоровых людей содержание литохолевой, дезоксихолевой, хенодезоксихолевой, холевой и дегидрохолевой кислот в среднем составляет 0,50; 1,25; 3; 80; 2,26; 0,22мг/мл.
Исследование литолитических свойств некоторых производных холановых кислот
После проведенного лечения хенодезоксихолевои кислотой у больных повысилось содержание дезоксихолевой кислоты-до 13,1%), а хенодезоксихолевои до 28,13%, в то же время снизилось количество холевой кислоты-до 25,12%).
Существуют данные [70-71], о том, что отруби неизменно влияют на химизм желчи, то есть они снижают количество дезоксихолатов в желчи приблизительно вдвое, что компенсировалось повышением хенодезоксихолатов.
В процессе хено-урсотерапии постепенно возростало содержание всех холановых кислот и особенно Зсс,7а-дигидроксихолановой кислоты в то же время концентрация холевой кислоты снизилось до контрольных величин.
Газохроматографические исследования желчных кислот желчи больных желчнокаменной болезнью на фоне введения урсодезокси и хенодсзоксихолевой кислот, показало преобладание хенодезоксихолевой кислоты при одновременном снижении концентраций дезоксихолевой, дегидрохолевои и холевой кислот, свидетельствующие о восстановлении желчно-кислотного метаболизма.
Терапия урсодезоксихолевой кислотой, кроме холевой и дезоксихолевой кислот несколько снижает синтез эндогенной хенодезоксихолевой кислоты [72].
Одним из перспективных методов лечения желчнокаменной болезни является растворение камней химическим способом, вследствие применения различных безвредных для организма растворителей.
Растворимость желчных камней зависит, прежде всего, от их структуры и химического состава. Если холестериновые и пигментные камни можно растворить без особых трудностей, то этокальциевые (рентгеноконтрастные); кальцинированные холестериновые камни часто не поддаются полному растворению. Тем не менее, при сочетании цитрата с дезоксихолатом растворимость этих камней значительно увеличивается.
Рядами авторов было доказано, что при введении в организм хенохола уменьшается литогенность желчи [73]. В результате чего наблюдается торможение синтеза холановых кислот из холестерина, т.е. снижение активности гидрокси-3-метилглутарил-Со-редуктазы в печени (фермент, который участвует в синтезе холестерина). Позднее это положение было подтверждено многими авторами [74-75]. При желчнокаменной болезни значительно возрастает синтез холестерина, а значит, и его поступление в желчь и плазму [76].
Использование хено- и урсодезоксихолевых кислот в терапии желчнокаменной болезни является наиболее безопасным, однако самым медленным и наиболее дешевым, в то же время наименее инвазивным из всех нехирургических подходов продолжая сохранять свою актуальную значимость в современной терапии желчнокаменной болезни.
У пациентов, прошедших специальный отбор, этот метод лечения оказывает достаточный эффект, а побочные действия легко подаются коррекции [77,78,79].
Использование всего многообразия некоторых стероидов возможно лишь при глубоких знаний их структуры, физических и химических свойств. Это предлагает не только разработку метода синтеза соединений заданных структур, но и всестороннее изучение их превращений.
Развитие синтетических работ в этом направлении диктуется также потребностью народной медицины в веществах с отчетливо выраженной биологической активностью, которая присуща многим классам стероидных соединений.
Всесторонная обработка литературных данных по синтезу и свойствам холановых кислот, а также проведенныю целенаправленных реакций протекающих по карбоксильным, гидроксильным и кетонным группам изучена, весьма ограничено. Это зачастую не позволяет сделать однозначные обоснованные выводы об их реакционной способности и направленности тех или иных реакций и т.п.
Поэтому выбор этого направления работы, ее актуальность объясняется также тем, что в литературе имеется весьма мало сведений о выделении и определении холановых кислот, а также о синтезе препаратов, растворяющих холестериновые желчные камни в желчном пузыре и желчных протоках.
Резюмируя литературные данные по растворению холестериновых камней желчного пузыря и желчных протоков, по нашему мнению можно сказать, что растворенние желчных камней является самостоятельным методом лечения. В то же время проблема поиска препаратов, растворяющих холестериновые и другие виды камней остаётся- по-прежнему, одной из актуальных проблем для ученым, проводящими исследования в этой области.
Необходимо важно отметить, что задачей проводимых работ является нахождение путей использования природных холановых кислот с целью синтеза биологически активных соединений, пригодных для лечения печени и желчнокаменной болезни.
Разработанные методы синтеза могут быть использованы при целенаправленном получении новых производных холановых кислот и они в дальнейшем могут найти применение в качестве лекарственных препаратов, в частности, как препараты препаратов растворяющие холестериновые желчные камни.
Изучение реакции гидрозидирования холановых кислот
Одним из перспективных методов лечения по удалению желчных холестериновых камней является растворение камней химическими способом. Поэтому поиск препаратов, растворяющих желчные камни, остаётся по-прежнему одной из важных задач синтетической органической химии.
В качестве потенциально биологически активных веществ представляет интерес также функциализация холановых кислот путём введения по карбоксильной и гидроксильной группам остатков различных органических соединений [93,94,95].
Продолжая поиск по изысканию новых биологически активных веществ в ряду функциональных производных холановых кислот, нами были проведены исследования по разработке препаративных методов синтеза гидразидов на основе пропиловых эфиров холановых кислот.
В этом плане представлялось интересным исследовать поведение пропиловых эфиров За,7а,12а-тригидрокси-, За,7а-диацето-12-гидрокси-, За,7а-диацето-12-кето-, За,7а-дигидрокси-12-кето- и За,7а,12а-трикетохолановых кислот в реакциях гидразидирования.
Для решение этой задачи, нами были разработаны препаративные методы синтеза гидразида-За,7а,12а-тригидрокси-(ХХУШ), гидразида-За,7а -диацето-12а-гидрокси-(ХХ1Х), гидразида За,7а-диацето-12-кето-(XXX), гидразида-3а,7а -дигидрокси-12-кето-(ХХХ1), гидразида-3а,7а,12а-трикето-(ХХХП) и За,7а-дигидроксихолановой кислоты (XXXIII); перечень соединений, выход в %, температуры плавления и данные элементного анализа которых приведены в таблице 7.
Поиск оптимальных условый реакции гидразидирования показал, что рассматриваемые вышеприведенные исходные пропиловых эфиров легко подвергаются гидразидированию в среде пропилового спирта при температуре кипения растворителя, с использованием гидразингидрата - в качестве гидразидированного агента [96]. Реакцию гидразидирования осуществляли по следующей схеме.
Анализ ИК-спектров, газожидкостной и аналитической тонкослойной хроматографии, а также данные элементного анализа гидразидов показывают, что при проведении реакции гидразидирования различных полифункциональпроизводных пропиловых эфиров холановых кислот, каких-либо побочных реакций не происходит. В ИК-спектрах полученных гидразидов ХХУШ-ХХХШ) присутствуют характерные полосы поглощения валентных колебаний гидроксильных групп при 3450-3460 см"1, кетонных групп 1770-1800см" , ацетильных групп 1340-1350 см"1, а также интенсивные полосы поглощения №І2-группьі в области 3380-3550см".
Индивидуальность синтезированных гидразидов-(ХХУШ-ХХХШ) проверялась хроматографией на тонком закреплённом гипсом слое силикагеля АСК. В качестве элюента использовали систему хлороформ:этанол-9:1, проявитель пары йода.
Таким образом, нами было исследовано поведение различных функциональпроизводных пропиловых эфиров холановых кислот в реакции гидразидирования и показано, что проведение таких реакций вполне осуществимо, на основе которых можно получать многочисленные производные холановых кислот как потенциальных биологически активных соединений.
В синтетической органической химии большую перспективу также имеют исследования, направленные на изучение свойств холановых кислот, включающих остатки некоторых серосодержащих гетероциклических соединений.
Это объясняется тем, что аналогичные молекулы, имея в своем составе фрагменты обладающие сильной биологической активностью, могут проявлять более усиленный эффект либо проявлять неизвестную ранее биологическую активность.
Можно предположить, что аналогичные исследования имеют реальную перспективу в создании препаратов для профилактики и лечения болезней печени и желчевыделительной системы.
Известно, что решающее значение в этиологии желчнокаменной болезни имеет нарушение нормального метаболизма холестерина и его производных холановых кислот-[97]. С другой стороны, те же самые кислоты и их аналоги, в ряди случаев, могут служить эффективными средствами для лечения желчнокаменной болезни-[98-99].
Следует, подчеркнуть, что при этом важнейшей составной частью таких исследований, несомненно, является поиск и нахождение путей использования природных холановых кислот для получения (биологически активных соединений, пригодных для лечения желчнокаменной болезни, а также проявляющих другие виды активности. При этом важное значение имеет выявление зависимости между строением веществ и их биологической активностью.
Все это указывает на перспективность развития всесторонных исследований по выявлению существующей связи между химие холановых кислот и гетероциклических соединений, включая методы их трансформации и определения.
С целью синтеза некоторых серосодержащих стероидов (типа холановых кислот), обладающих более сильной биологической активностью нами был предпринят целенаправленный синтез ряда кетостероидов соответствующего строения, для того чтобы включить фрагменты гетероциклических соединений.
Для выполнения данной задачи было предпринята попытка синтеза За,12а-дигидрокси-7-кетометилхолата-(ХХХ1У) и других кетостероидов по [100].
Известно [101], что в холановых кислотах гидроксил при углероде 3 экваториален, остальные гидроксилы аксиальные. Экваториальный гидроксил ацилируется гораздо легче, чем аксиальный, поэтому он может быть защищен ацилированием и наоборот, окисляется он труднее. Наиболее легко окисляется аксиальный гидроксил в положение 7, поэтому при осторожном окислении его можно окислить до кетона. Используя этот метод, мы окислили За,7а,12а-тригидрокси холановую кислоту путём растворения его в растворе уксусной кислоты и далнейшей обработке раствором хромата калия
Влияние За,7а-дигидроксихолановой кислоты на физико-химические свойства дестабилизированной желчи
В литровую плоскодонную колбу добавляют Юг За, 12а-дигидроксихолановой кислоту в 26мл ледяной уксусной кислоты. После растворения продуктв к смеси добавляют раствор 7г хромата калия (К2СЮ4) в 20мл дистиллированной воды. Реакционную смесь, взбалтывают, и оставляют при температуре 25 С в течение 12 часов.
После чего содержимое колбы разбавляют водой до помутнения раствора. Выпавший осадок отфильтровывают, затем промывают водой до (рН=7) нейтральной реакции. Осадок подвергают сушке и перекристаллизировывают из этанола. Выход За-гидрокси-12а-кетохолановой кислоты составляет 9,5г (97%).Т.пл.192-193С. Найдено: % С 73,67; Н9,68 Вычислено для С24Н38О4: % С 73,80; Н 9, Смешивают Юг За-гидрокси-12-кетохолановой кислоты с 3,5г гидразингидрата (85%), прибавляют 5,6г растворенного едкого калия в 27мл этиленгликоля.
Смесь кипятят в течение 2 часов с обратным холодильником. Затем соединяют колбу с нисходящим холодильником и медленно отгоняют смесь гидразингидрата и воды, пока температура реакционной смеси не поднимается до 195 С. Температуру поддерживают до прекращения выделения азота.
После охлаждения реакционную смесь разбавляют равными объёмами воды и подкисляют концентрированной соляной кислотой до рН=3. После чего несколько раз экстрагируют бензолом или этилацетатом. Растворитель промывают и сушат сульфатом натрия. После отгонки растворителя осадок перекристаллизовывают из этилового спирта. Выход 9,5г(89%). Т.пл. 184-185С. Найдено: % С 78,38; Н 10,49
Вычислено для С24Н40О3: % С 76,46; Н 10, В круглодонную колбу, снабженную обратным холодильником, помещают 20гр За,7а-диацето-12-кетометилхолата с 7г гидразингидрата, прибавляют 11,2г растворенного едкого калия в 55мл этиленгликоле. Смесь кипятят в течение 2,5 часов с обратным холодильником. Затем соединяют колбу с нисходящим холодильником и медленно отгоняют смесь гидразина и воды, пока температура реакционной смеси не поднимется до 195С. Температуру поддерживают до прекращения выделения азота. После охлаждения реакционную смесь разбавляют равным объёмом воды и подкисляют концентрированной соляной кислотой до рН=3. Затем несколько раз экстрагируют этилацетатом. Экстракт промывают водой и сушат сульфатом натрия. После удаления растворителя осадок многократно перекристаллизовывают из этилового спирта. Выход 12г(68%). Т. пл. 140-141С. Найдено %: С 73,50, 73,62; Н 10,11, 10,29
Вычислено для СгДікА0/": С 73,36; Н 10, 5г (0,012мол) За,7а,12а-тригидроксихолановой кислоты растворяют в 200мл уксусной кислоты, обрабатывают 28,5г (0,14моля) хромата калия (К2СЮ4) в 90мл дистиллированной воды и оставляют при 25С на 24 часа. После чего реакционную массу разбавляют до помутнения водой, образовавшийся осадок отфильтруют и промывают водой до нейтральной реакции (рН=7). Полученный осадок перекристаллизовывают из этилового спирта. Выход 4,1 г (98%) Т.пл. 237-238С. Найдено %: С 71,60, 71,69; Н 8,51,8,49
Вычислено для С24Н34О5 %: С 71,64; Н 8, В круглодонную колбу помещают ЮОг (0,25моля) За,7а,12а-тригидроксихолановой кислоты и растворяют в 300мл метанола. Затем добавляют 4мл концетрированной соляной кислоты, и смесь кипятять с обратным холодильником и хлоркальциевой трубкой в течение 20 минут. Реакционную колбу оставляют на ночь, затем фильтруют и сушат при 100 С в термостате. Продукт перекристаллизовывают из метанола. Выход 97г (93%). Т. пл. 156-157С. Найдено %: С 71,02, 71,08; Н 9,79, 9,81 Вычислено для С24Н4205 %: С 71,10; Н 9,94 Аналогичным образом были синтезированы метиловые эфиры других холановых кислот (VI, VII, VIII, Х,Х1) см. табл. 2.