Содержание к диссертации
Введение
1. Пути переработки возгонов электроннолучевого переплава ниобия 10
1.1. Формирование возгонов электроннолучевого переплава ниобия 10
1.2. Пирометаллургические способы переработки 12
1.2.1. Термодинамический анализ процесса выплавки феррониобия из возгонов 12
1.2.2. Экспериментальная проверка плавки возгонов на феррониобий 15
1.2.3. Испытания технологии плавки возгонов на феррониобий в печи ЭШП 17
1.3. Гидрометаллургические и комбинированные способы переработки 18
1.4. Выводы 22
2. Исследование процесса окисления возгонов 23
2.1. Методика и объект исследований 23
2.2. Исследование микроструктуры и распределения элементов по фазовым составляющим возгонов 24
2.3. Окисление возгонов на воздухе 33
2.3.1. Термический анализ взаимодействия возгонов с кислородом воздуха 33
2.3.2. Кинетические особенности процесса 41
2.3.3. Влияние температуры и продолжительности на полноту окисления и фазовый состав продуктов 47
2. 4. Реагентное окисление возгонов 50
2.4.1. Термодинамическое моделирование взаимодействия NbAl3
с оксидными соединениями Na и Са 50
2.4.2. Термические исследования и выбор реагента для окисления возгонов 57
2.4.3. Оптимизация параметров окисления возгонов с карбонатом натрия 65
2.5. Выводы 78
3. Исследование процессов выщелачивания продуктов обжига-спекания возгонов 80
3.1. Методика исследований 80
3.2. Водно-щелочная обработка спека 81
3.2.1. Термодинамическое моделирование процесса 82
3.2.2. Экспериментальные исследования и оптимизация параметров водно-щелочной обработки 84
3.3. Кислотное выщелачивание щелочного кека 88
3.3.1. Обоснование выбора кислоты 88
3.3.2. Термодинамическое моделирование процесса 90
3.3.3. Математическое моделирование и оптимизация процесса 93
3.3.4. Кинетика процесса кислотного выщелачивания 106
3.4. Выводы 114
4. Укрупненно-лабораторные испытания технологии переработки возгонов 116
4.1. Схема переработки возгонов по комбинированной технологии 116
4.2. Оценка возможности плавки ниобатного концентрата на черновой ниобий и феррониобий 118
4.3. Переработка возгонов на пентаоксид ниобия 127
4.4. Выводы 131
Заключение 132
Список использованных источников 135
Список опубликованных работ 144
- Гидрометаллургические и комбинированные способы переработки
- Исследование микроструктуры и распределения элементов по фазовым составляющим возгонов
- Экспериментальные исследования и оптимизация параметров водно-щелочной обработки
- Оценка возможности плавки ниобатного концентрата на черновой ниобий и феррониобий
Введение к работе
Актуальность работы
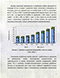
При рафинировочных электроннолучевых переплавах (ЭЛП) чернового ниобия, полученного внепечным алюминотермическим или алюмино-кальцийтермическим восстановлением Nb2O5, значительное количество ниобия переходит в возгоны. Содержание ниобия в возгонах ЭЛП зависит от исходного состава и стадии переплава чернового ниобия. При рафинировании металла, полученного алюминотермическим и алюмино-кальцийтермическим восстановлением Nb2O5, содержание ниобия в возгонах первого ЭЛП не превышает 15% и 50%, соответственно. В возгонах последующих переплавов концентрация ниобия возрастает до 60-90%.
Богатые ниобием возгоны второго и последующих переплавов возвращают в процесс восстановления Nb2O5. Из-за необходимости вывода примесей бедные возгоны ЭЛП нельзя вводить в шихту металлотермической выплавки ниобия. Гидрохимическая переработка возгонов ЭЛП совместно с рудным сырьем (ниобиевые, тантал-ниобиевые концентраты, шлаки и др.) осложнена особенностями поведения компонентов возгонов при их кислотном растворении.
В этой связи изучение технологических возможностей переработки возгонов ЭЛП на полуфабрикат ниобия, пригодный для использования в технологии получения слитков ниобия, или на готовую продукцию представляет как научный, так и практический интерес.
Целью диссертационной работы является физико-химическое обоснование пиро- и гидрометаллургических технологий извлечения ниобия из возгонов электроннолучевого переплава чернового ниобия.
Для достижения указанной цели решены следующие задачи:
- выявлена особенность структуры и фазового состава возгонов;
- проверена возможность пирометаллургической переработки возгонов на феррониобий;
- исследовано окисление возгонов кислородом воздуха, обоснован реагент для интенсификации этого процесса;
- определены оптимальные технологические параметры окислительного обжига-спекания возгонов с карбонатом натрия и условия гидрохимического концентрирования ниобия;
- разработана и опробована комбинированная пиро-гидрохимическая схема извлечения ниобия из возгонов в химический концентрат.
Научная новизна работы заключается в том, что:
- выявлены ниобийсодержащие фазы возгонов (алюминид NbAl3; силицид Nb5Si3; карбид NbСх);
- получены сведения о фазовых превращениях при взаимодействии возгонов и его основной фазы - NbAl3 с оксидами Fe2O3, CаO2 и карбонатами Na2CO3, СaCO3, а также обоснованы возможности плавки возгонов с извлечением ниобия в феррониобий и окислительного обжига-спекания возгонов с переводом ниобия и алюминия в натриевые соли, а металлов-примесей (Si, Fe, Cr и др.) в оксиды Na2О MеOх;
- построены многофакторные математические модели для оптимизации параметров и прогнозирования показателей процесса концентрирования ниобия в полуфабрикате (технический NaNbO3) при гидрохимической обработке спека.
Практическая значимость работы заключается в том, что:
- предложены и проверены пирометаллургическая технология извлечения ниобия из возгонов ЭЛП в ферросплав и комбинированная пиро-гидрохимическая схема переработки возгонов на химический концентрат, пригодный для получения чернового ниобия.
Работа выполнена в рамках программы аспирантской подготовки и тематических планов ИМЕТ УрО РАН, а также программы ОХНМ РАН (№ 09-Т-3-1019) и при поддержке министерства образования и науки РФ (госконтракт № 02.740.11.0821).
На защиту выносятся результаты:
- изучения вещественного, фазового состава возгонов;
- исследований и испытаний пирометаллургической переработки возгонов с извлечением ниобия в феррониобий;
- экспериментального определения оптимальных режимных параметров процессов обжига-спекания возгонов и водно-щелочной обработки спека;
- разработки многофакторных математических моделей сернокислотного выщелачивания кека, полученного после водно-щелочной обработки спека, позволяющих прогнозировать технологические показатели и оптимизировать режимные параметры процесса;
- укрупненно-лабораторных испытаний предлагаемой принципиальной технологической схемы переработки возгонов на полуфабрикат ниобия.
Публикации и апробация работы
Материалы диссертационной работы изложены в 12 статьях, опубликованных в российских и зарубежных научных журналах и сборниках, в тезисах 8 докладов на международных и всероссийских научных конференциях.
Результаты работы были представлены на I Международной научной конференции «Диффузия в твердых и жидких материалах» (Португалия, 2005), II Международной научной конференции «Диффузия в твердых и жидких материалах» (Португалия, 2006), Международной научно-технической конференции «Научные основы и практика переработки руд и техногенного сырья» (Екатеринбург, 2008), IV Международной научной конференции «Диффузия в твердых и жидких материалах» (Испания, 2008), Европейской Металлургической конференции «EMC2009» (Австрия, 2009).
Структура и объем диссертации
Гидрометаллургические и комбинированные способы переработки
Попытки прямого растворения возгонов смесями серной и плавиковой кислот были предприняты сотрудниками ОАО «Уралредмет». Как показали результаты испытаний, максимальное извлечение ниобия в раствор не превышало 85%. Причина низкого извлечения не только в трудновскрываемых алюминидах ниобия, но и в известной устойчивости к действию кислот карбида ниобия [6], который присутствовал в возгонах ЭЛП. Он образуется на стадии выплавки чернового ниобия, благодаря контакту расплава металла с графитовыми изложницами в печи восстановления Nb2Os. Из этого следует, что переработка бедных возгонов по сульфатно-фторидной технологии без предварительного окисления неэффективна.
Для оценки применимости известных технологий переработки ниобиевых рудных концентратов для извлечения ниобия из предварительно окисленных возгонов рассмотрим следующие способы. 1. Разложение сырья растворами минеральных кислот на основе фтористоводородной кислоты (HF, HF+H2S04, HF+HNO3) или на основе серной кислоты (H2SO4 или H2S04+ (NH4)2S04). В первом случае в результате разложения концентрата ниобий извлекают в раствор, из которого методом экстракции получают оксиды ниобия [9]. Во втором - ниобий извлекают в сернокислотные растворы, из которых в результате ряда переделов получают индивидуальные соединения элементов или оксиды ниобия [10-11].
На ОАО «Силмет» (Эстония) возгоны перерабатывают вместе с рудным сырьем. Для этого измельченные возгоны ЭЛП предварительно окисляют во вращающихся трубчатых печах ВНД-6 при температурах 900-1000С в атмосфере воздуха в несколько стадий, а затем добавляют к рудным концентратам, перерабатываемым по фторидно-экстракционной технологии на пентаоксид ниобия. Процесс окисления характеризуется низкой степенью превращения основных компонентов возгонов в оксиды, что снижает эффективность их использования.
Следует отметить, что процессы кислотного вскрытия осуществляют при температурах 80-130С и высоких концентрациях кислот, что сопровождается образованием токсичных паров. Такой процесс требует дополнительных расходов на улавливание и регенерацию кислот. 2. Хлорирование ниобиевых концентратов с получением конденсата хлоридов и последующим их гидролитическим разложением с получением оксида ниобия.
Способ хлорирования применяют на ОАО «Соликамский магневый завод» для переработки лопаритового концентрата [5, 12, 13]. Сущность способа заключается в том, что при повышенной температуре взаимодействие компонентов сырья с газообразным хлором в присутствии восстановителя металлов приводит к образованию хлоридов. Различие давлений паров хлоридов позволяет разделить металлы методом фракционной конденсации. При многих положительных характеристиках, таких как высокое извлечение всех полезных металлов, хорошие экономические показатели, хлорная технология имеет свои недостатки: сложность эксплуатации оборудования, необходимость утилизации хлоридных остатков и экологическая опасность технологии. 3. Сплавление (или взаимодействие в водных растворах) концентратов со щелочными реагентами и последующее водное и кислотное выщелачивание, с получением оксидов ниобия.
Сущность этого метода заключается в том, что при взаимодействии ниобиевого сырья с солями натрия образуются ниобаты, малорастворимые в воде и кислотах [4-5]. Алюминий и другие примеси переходят в раствор в виде натриевых солей. При последующей кислотной обработке растворяются соединения железа и марганца.
В схемах переработки различного вольфрамового сырья, содержащего ниобий и тантал, также используют спекание с солями натрия и последующее выщелачивание из спека вольфрамата натрия [14-15]. После гидрометаллургической обработки спека ниобий и тантал концентрируются в твердом остатке. При обработке кека соляной кислотой достигается перевод в раствор железа и марганца. Извлечение тантала и ниобия в концентрат достигает 96-100% [14-15]. Авторы отмечают, что такой способ характеризуется высокой эффективностью даже при переработке химически упорных концентратов, поскольку процесс взаимодействия с карбонатом натрия сопровождается обильным выделением СО2, оказывающим перемешивающее воздействие, что приводит к обновлению поверхности контакта между концентратом и расплавом и не позволяет твердым частицам слеживаться. Преимуществами описанного способа являются технологическая, аппаратурная простота и экологическая безопасность [14].
Из рассмотренных способов наиболее рациональным направлением переработки окисленных возгонов ЭЛП ниобия представляется спекание возгонов с натрийсодержащими солями и последующее гидрохимическое концентрирование ниобия.
Логично заключить, что для переработки богатых возгонов с содержанием ниобия более 45% следует использовать плавку на феррониобий, а для бедных возгонов наиболее перспективной может оказаться пиро-гидрометаллургическая технология.
В качестве примера успешного применения комбинированных технологий можно рассматривать переработку металлотходов сверхпроводящих материалов, состоящих либо из сплава Nbi, либо из интерметаллида Nb3Sn в медной или бронзовой матрицах [16]. В результате окислительной плавки сырья с карбонатом и (или) сульфатом натрия при температуре 1100-1150С получают медный продукт и щелочной ниобийсодержащий шлак (плав), который подвергают водно-кислотной обработке. Последовательная обработка плава водой и затем серной кислотой позволяет получать продукт, близкий по содержанию ниобия к ниобату натрия.
Исследование микроструктуры и распределения элементов по фазовым составляющим возгонов
Исследования выполнены на возгонах первого переплава чернового ниобия (табл. 7 образец 2), основу которых составляет интерметаллид NbAl3 и металлический алюминий (рис. 6), что соответствует данным диаграммы состояния системы Nb-Al по ряду источников [19-21]. Помимо этого идентифицированы слабые рефлексы карбида ниобия.
Для данного образца возгонов характерно формирование структур двух типов - слоистой и дендритной, что, вероятно, связано с условиями ведения процесса рафинирования ниобия и влиянием различных факторов на кристаллизацию сублимата.
На рисунке 7 представлен общий вид участка слоистой структуры, на котором четко выражено чередование темных и светлых фаз. Толщина слоев изменяется от 30 до 1 мкм. Наибольшую толщину имеют темные слои (рис.8-9), состоящие, согласно результатам рентгеноспектрального микроанализа (табл.8), преимущественно из металлического алюминия (точка 2). В них отмечены включения более светлой фазы (точка 1), содержащие элементы-примеси. Ее состав (%: 66,97 А1, 19,14 Fe, 7,09 Si, 3,26 Mn, 2,84 Сг) при некотором избытке алюминия, близок к соединению Al5FeSi, которое, по имеющимся литературным сведениям, свойственно системе Al-Fe-Si [22-24]. Вероятнее всего, рассматриваемая фаза является эвтектикой Al+Al5FeSi, кристаллизованной в виде дисперсных дендритов (точка 1).
Известно [25-26], что присутствие Mn и Cr даже в небольших количествах приводит к образованию фаз переменного состава oc-AlFeSiMn(Cr), поэтому, можно ожидать, что и в нашем случае примеси концентрируются в соединениях подобного типа. Более светлые полосы характеризуются высоким содержанием ниобия. На кривых распределения по линии сканирования (рис.8) видно, что в самом светлом слое содержание ниобия доходит до 90%. Например, фаза в точке 3 состоит из 75,34% Nb и 20,92% А1, превышая отношение ниобия к алюминию в NbAl3, что дает основание предположить присутствие в возгонах Nb2Al.
При наблюдении микроструктуры при 3000 кратном увеличении (рис.9) отмечено чередование фаз внутри каждого слоя. Состав светло-серой фазы в точке 4 близок к эвтектике NbAl3+Nb2Al [19], а в точке 7 - к твердому раствору NbAl3+Al. В зоне темных полос, состоящих из алюминия, находятся участки, аккумулирующие железо и кремний. Судя по химическому составу, их можно отнести к твердым растворам на основе Al5FeSi (точка 5) и Al3Fe (точка 6).
Как уже отмечалось, возгоны ЭЛЛ ниобия характеризуются непостоянством как химического, так и фазового составов. Рассмотренная выше слоистая структура свойственна пористой части возгонов, представляющей основу материала. Микроструктура другого типа (рис. 10) дендритная - характерна для пластинчатых и округлых частиц с металлическим блеском, расположенных в порах или вкрапленных в слоистую часть возгонов. частиц возгонов (увел.200) Эта двухфазная структура (рис.11-12) по данным рентгеноспектрального микрозондирования (табл.9) состоит из светлых округлых дендритов алюминида ниобия NbAl3 (точки 4 и 8), между которыми располагается темная фаза, близкая по составу к Al8Fe2Si [26]. В междендритном пространстве найдены включения черного цвета, отнесенные к оксидной фазе на основе А1203 (точка 1), содержащей железо, кремний и никель. Судя по составу в точках 5 и 6, из темной фазы дендритной структуры кристаллизуются сложные твердые растворы, объединяющие как основные компоненты, так и примеси. На участках дендритов видны более светлые образования (точки 3 и 7), содержащие в сравнимых количествах Nb, Al, Fe и Si. Фаза ярко-белого цвета (точка 2) представляет собой силицид ниобия Nb5Si3 [27-29]. Следует отметить, что в структуре металлизированной части возгонов встречаются единичные частицы чистого металлического ниобия.
В результате проведенных исследований выявлено, что основной фазой, как и предполагалось, является интерметаллид NbAl3. Ниобий присутствует также в форме силицида - NbsSi3 и в виде сплава Nb-Al с содержанием Nb более 90%. Алюминий может находиться в возгонах в элементном виде, в твердом растворе с железом и кремнием или в виде оксида. Примесные элементы распределены между оксидной фазой на основе а-АІгОз (Fe, Si, Mg, P, Ca, Ni) и твердым раствором Al-Fe-Si (Cr, Mn, Ni).
В результате проведенных исследований выявлено, что основной фазой, как и предполагалось, является интерметаллид № А1з. Ниобий присутствует также в форме силицида - Nb5Si3 и в виде сплава Nb-Al с содержанием Nb более 90%. Алюминий может находиться в возгонах в элементном виде, в твердом растворе с железом и кремнием или в виде оксида. Примесные элементы распределены между оксидной фазой на основе а-А1203 (Fe, Si, Mg, Р, Ca, Ni) и твердым раствором Al-Fe-Si (Cr, Mn, Ni).
Окисление на воздухе NbAb — основы возгонов — достаточно подробно изучено в литературе [30-41], авторы отмечают сложный механизм окисления, состоящий из нескольких стадий. При температуре выше 1000С на поверхности интерметаллида начинает образовываться слой оксида алюминия с формированием на границе А12Оз-№ А1з низшего алюминида Nb2Al по реакции: 4NbAl3 + 7,502 = 5А1203 + 2Nb2Al (2) Окисление по уравнению (2) продолжается до тех пор, пока скорость диффузии алюминия через слой Nb2Al высока. По мере нарастания слоя Nb2Al массоперенос алюминия замедляется, что приводит к образованию быстрорастущих оксидных фаз за счет окисления Nb2Al по реакции: 2Nb2Al + 6,502 = Nb205 + 2NbA104. (3) Когда фаза Nb2Al полностью израсходована на образование NbA104, под оксидом начинает формироваться новый слой А12Оз и цикл повторяется, обуславливая послойное расположение продуктов реакции (2) и (3). Схематично этот процесс представлен на рисунке 13. Поскольку возгоны содержат кроме NbAl3 элементный алюминий, ниобий и ряд примесных элементов, то представляет интерес изучение их влияния на полноту окисления возгонов и скорость процесса.
Экспериментальные исследования и оптимизация параметров водно-щелочной обработки
Условия водно-щелочной обработки, выбранные по термодинамической модели, были проверены экспериментально. Для этого спек разделен на две фракции крупности -0,5 мм и 0,2 мм. Обработка водой отдельных фракций спека при 80С в течение 60 мин показало, что с увеличением отношения Ж:Т степень извлечения алюминия в кек снижается с 36,8% до 27,6% для фракции 0,5 мм и с 27,5% до 24,2% для фракции -0,2 мм (табл.18). Таблица 18 - Влияние крупности частиц (d) и отношения Ж:Т на водно-щелочную обработку спека (80С, 60 мин) Железо в обоих случаях переходит в щелочной кек вследствие гидролиза феррита натрия с образованием гидрооксида железа. Ниобий в виде ниобатов натрия практически полностью остается в твердом остатке. Степень извлечения кремния в щелочной кек повышается с увеличением отношения Ж.Т, что объясняется образованием труднорастворимого соединения - NaAlSi04-Максимальное удаление кремния достигается при крупности спека -0,2 мм и отношении Ж:Т = 3. Присутствие хрома в кеке снижается с увеличением отношения Ж:Т и крупности спека. Для более полного извлечения в раствор примесей при водно-щелочной обработки крупность частиц спека должна быть не более 0,2 мм, а отношение Ж:Т равное 4. При более низких отношениях Ж:Т затруднен перевод в раствор кремния. Эксперименты по изучению влияния температуры и продолжительности водно-щелочной обработки спека на степень извлечения элементов проводились при постоянных отношении Ж:Т = 4 и крупности частиц 0,2 мм. Температура и продолжительность обработки спека водой не влияют на поведение ниобия и железа — они практически полностью остаются в кеке (табл. 19 и 20). Извлечение в щелочной кек хрома и кремния с ростом температуры уменьшается с 40% до 27% и с 48% до 30%, соответственно.
Минимальная степень извлечения в кек алюминия (26%) достигается при температуре 80С и продолжительности 60 минут. Таким образом, оптимальные результаты водно-щелочной обработки продуктов окислительного обжига-спекания возгонов получены при ведении процесса в следующих условиях: - крупность менее 0,2 мм; - температура 80С; - продолжительность 60 мин. В данных условиях выделен щелочной кек, содержащий (масс.%) 26,7 Nb, 11,2А1, 2,8 Fe, 0,13 Si, и 0,078 Сг. По результатам РФА основными фазами является NaNb03, А1(ОН)3, А1203 (рис.42). Для более глубокого концентрирования ниобия рассмотрено кислотное удаление примесей Al, Fe, Si, иСг. По результатам рентгенофазового анализа основными компонентами кека после водно-щелочной обработки спека являются метаниобат натрия, гидрооксид и оксид алюминия (рис.42). На основании литературных данных элементы-примеси (алюминий, кремний, железо и хром), присутствующие в щелочном кеке в малом количестве, могут находиться в виде следующих соединений: Na20-Al203-2Si02-2H20, Fe203, NaA102, А1203-Н20, Al(OH)Cr04-H20, Cr203 HNaCr02. Как известно [86-88], ниобаты и хромит натрия устойчивы к действию кислот. Оксиды алюминия и железа растворяются в кислотах с образованием соответствующих солей. Следовательно, в ходе кислотного выщелачивания щелочного кека примеси алюминия, железа и хрома должны переходить в раствор, а ниобий -концентрироваться в твердом остатке. Для сравнения эффективности удаления примесей при кислотном выщелачивании использовали растворы серной, азотной и соляной кислот. Результаты выщелачивания щелочного кека, показали (табл.21), что максимальный перевод примесей в раствор достигается при использовании соляной кислоты (концентрация 18%). Однако при этом потери Nb с растворами составили 2%. При использовании концентрированных растворов соляной кислоты образуются коллоидные растворы, что затрудняет процесс фильтрации.
При выщелачивании серной кислотой в раствор переходит 0,3% Nb, но концентрирование в твердом остатке железа и кремния выше, чем при выщелачивании соляной кислотой. С азотной кислотой в раствор переходит до 4,5% Nb и перевод основных примесей в раствор относительно низкий. При использовании для выщелачивания кека смесей кислот результаты оказались на том же уровне или ниже по сравнению с действием отдельно взятой кислоты (табл.22). Добавление НС1 к растворам H2S04 позволяет снизить содержание в концентрате Fe, А1, но возрастают потери с раствором ниобия. Смеси с азотной кислотой менее активно растворяют соединения Fe и А1 при заметных потерях ниобия. Исходя из анализа проведенных экспериментов, для кислотного выщелачивания кека водно-щелочной обработки спека выбрана серная кислота, позволяющая избежать потерь ниобия с растворами. Для прогнозирования влияния основных параметров выполнен термодинамический анализ сернокислотного выщелачивания кека водно-щелочной обработки спека. В расчете использовали усредненный состав кека, масс. %: 50 NaNb03, 36,7 А1203 ЗН20, 4 Fe203, 0,5 Si02, 0,1 NaCr02. В ходе моделирования оценивали влияние на равновесный состав продуктов выщелачивания отношения Ж:Т (рис.43) и температуры (рис.44). Зависимости равновесных составов фаз от отношения Ж:Т определены для ведения процесса при температуре 80С и концентрации серной кислоты 20%. По расчетам равновесных составов фаз можно утверждать, что с увеличением отношения Ж:Т в твердом остатке растут содержания NaNb03, Fe203 и Si02 и снижаются - А1203 Н20 и Сг02 (рис. 43). С ростом температуры (рис.44) следует ожидать повышение содержания в твердом остатке железа, полного растворения хрома и алюминия. Содержание метаниобата натрия в твердом остатке должно снизиться на 2-3%, а кремний остается без изменений.
Оценка возможности плавки ниобатного концентрата на черновой ниобий и феррониобий
Для термодинамического моделирования выплавки чернового ниобия в расчетах использован состав шихты, который используют на действующих предприятиях по производству металлического ниобия: 100 кг химического концентрата, 17 кг металлического алюминия, 25 кг металлического кальция. Состав химического концентрата, полученного в лабораторных условиях из возгонов масс.%: 92 NaNb03, 5,2 А1203, 0,1 Fe203, 0,2 Si02.
По результатам расчетов равновесных составов продуктов алюмино-кальцийтермического восстановления полученного химического концентрата при 1800С достигается максимальное извлечение ниобия - 98% (рис.53). Потери ниобия со шлаком в виде NbO объясняются недостатком восстановителя, поскольку некоторое его количество расходуется на восстановление натрия, находящегося в составе метаниобата NaNbCb — основы химического концентрата.
Для оптимизации состава шихты рассмотрено влияние на процесс расходов алюминия и кальция. Установлено, что с увеличением расхода алюминия до 20-22% (при 25% Са) потери ниобия снижаются с 1,0 до 0,1% (рис.54). Повышение расходов кальция до 30% (при 17% А1) позволяют сократить потери ниобия со шлаком до 0,3% (рис.55). Ожидаемые содержания примесей алюминия (до 2%), железа (0,1%) и кремния (0,3%) в металлической фазе соответствуют требованию к черновому металлу, и указывают на возможность использовать химический концентрат для выплавки чернового ниобия.
Моделирование плавки химического концентрата на феррониобий показало, что максимум извлечения ниобия в сплав (99%) при температуре 1650С лежит в области расходов восстановителя - алюминия 35-40% (рис.56). Расходы окалины заметно влияют только на содержание в сплаве алюминия (рис.57). В интервале расходов восстановителя 36-40% и Fe20317% содержание примесей в сплаве соответствует ГОСТ на феррониобий марки Фнб 60 (высший сорт) и международным стандартам ISO, ASTM (США) и JIS G 2319-61 (Япония) на феррониобий.
В ходе исследований процесса обжига-спекания возгонов с избытком карбоната натрия (раздел 2.4.3) обнаружено присутствие в продуктах взаимодействия ортониобата натрия - Na3NbC 4. Как известно, ортониобат натрия, растворяясь в воде, подвергается гидролизу с осаждением гексаниобата натрия (реакция необратима) [73]:
В растворах кислот гексаниобат натрия 7Na206Nb205-32H20 разлагается с образованием гидратированных оксидов ниобия 6Nb205 хН20 (64), при прокаливании (600-700С) которых образуется пентаоксид ниобия (65) [4].
Таким образом, изменение режима окисления возгонов ЭЛП ниобия позволяет концентрировать ниобий в виде химического концентрата на основе пентаоксида. Для исследований приготовили плав — продукт окисления возгонов с карбонатом натрия при температуре 1000С, выдержке 240 мин, отношении возгонов к карбонату натрия 1 : 2 (с учетом образования ортониобата натрия) в режиме сплавления. Химический состав используемых возгонов, %: 25,3 Nb, 51,7 А1, 2,9 Fe, 0,8 Si, 0,3 Сг. Химический состав полученного плава, %: 11,4 Nb, 22,3 А1, 1,04 Fe, 0,23 Si, 0,074 Cr.
При исследовании влияния основных параметров на процесс водно-щелочной обработки плава установлено, что с повышением температуры и продолжительности растет извлечение примесей в раствор (табл.40-41). Ниобий и железо при этом остаются в кислотном кеке. Максимальное удаление примесей достигается при температуре 80С и продолжительности водно-щелочной обработки 60 минут. Полученный в оптимальных условиях щелочной кек, содержит, %: 67 Nb205, 17 А1203, 4,1 Fe203, 0,4 Si02 и 0,1 Сг203.
Для сравнения эффективности удаления примесей при кислотном выщелачивании щелочных кеков опробовали растворы серной, азотной и соляной кислот, а также их смеси (табл.42). Использование соляной кислоты обеспечивает практически полное концентрирование ниобия.в твердом остатке (98,9%) и удовлетворительный переход железа и кремния в раствор. При обработке щелочного кека серной кислотой содержание железа в твердом остатке значительно выше. При выщелачивании с азотной кислотой возрастают потери ниобия с раствором до 4%. Добавление НС1 к растворам H2SO4 позволяет снизить содержание в концентрате Fe, А1. Смеси с азотной кислотой менее активно растворяют соединения Fe и А1 при заметных потерях ниобия. Исходя из анализа проведенных экспериментов, для кислотного выщелачивания щелочного кека выбрана смесь серной и соляной кислот, позволяющая избежать потерь ниобия с растворами (табл.42).